问题描述:
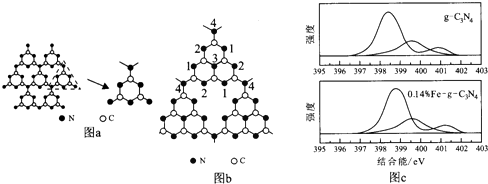
哈佛大学A.Y.Liu教授首次合成类金刚石相氮化碳(β--C3N4).福州大学王新晨教授在此基础上以单氰胺(CH2N2)为原料制得光催化剂类石墨相氮化碳(g-C3N4),其单层结构如图a,
(1)C、H,N元素电负性从大到小的顺序为___(填元素符号).
(2)β--C3N4熔点、硬度均高于金刚石,其原因为___.
(3)β--C3N4和g--C3N4中碳原子的杂化轨道类型分别为___.
(4)单氰胺的结构式为___.
(5)g--C3N4中存在的作用力为___(填序号).
a.离子键 b.σ键 c.π键 d.氢键 e.范德华力
(6)g--C3N4中掺杂少量铁元素能提高光催化效果.图b为g--C3N4的另一种单层结构;图c为Fe3+掺杂前后N-1s谱图(N原子1s的XPS谱图,图中峰的强度正比于原子数目),图c中横坐标为g--C3N4中N-1s结合能(原子结合能与稳定性成正比),掺杂Fe3+后,结合能最小的谱线发生了明显右移.
①Fe3+的价电子轨道表示式为___.
②发生位移的谱线对应的N原子为___(填图b中的序号).
③谱线右移的原因为___.
(1)元素的非金属性越强,其吸引电子能力越强,则其电负性越大,这几种元素非金属性强弱顺序是N>C>H,所以电负性大小顺序是N>C>H,故答案为:N>C>H;
(2)原子晶体熔沸点、硬度与键长成反比,β--C3N4是原子晶体,C-N原子之间形成共价键,且C-N键长小于C-C,则键能更大、熔点高硬度大,
故答案为:β--C3N4和金刚石都是原子晶体,C-N键长小于C-C,键能更大,熔点高硬度大;
(3)β--C3N4中C原子价层电子对个数是4、g--C3N4中碳原子价层电子对个数是3且不含孤电子对,根据价层电子对互称理论判断C原子杂化方式分别为sp3、sp2,故答案为:sp3、sp2;
(4)单氰胺N原子形成3个共价键、H原子形成1个共价键、C原子形成4个共价键,据此书写其结构式为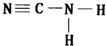 ,
,
故答案为: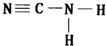 ;
;
(5)g--C3N4是分子晶体,非金属元素之间形成的共价单键为σ键、共价双键中一个是σ键、一个是π键,分子晶体中分子之间存在范德华力,C和N原子之间存在共价共价单键和共价双键,故选bce;
(6)①Fe原子失去3个电子生成Fe3+,其3d电子为价电子,其价电子轨道表示式为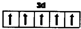 ,
,
故答案为: ;
;
②Fe3+与N原子形成配位键导致谱线发生移动,而图中1,2号N原子含有对孤对电子,能形成配位键,
故答案为:1,2;
③掺杂后Fe3+与N原子形成配位键,N原子周围的电子云密度降低,原子核对核外导致的束缚能力提高,0.14%Fe-g-C3N4样品中N-1s轨道结合能升高,故谱线右移.
故答案为:掺杂后Fe3+与N原子形成配位键,N原子周围的电子云密度降低,原子核对核外导致的束缚能力提高,0.14%Fe-g-C3N4样品中N-1s轨道结合能升高.

