问题描述:
下列是某化学研究性学习小组对某无色水样成分的检验过程,已知该水样中只可能含有K+、Mg2+、Fe3+、Cu2+、Ag+、Ca2+、CO| 2- 3 |
| 2- 4 |
①水样中一定含有的阴离子是___.
②试根据实验结果推测K+是否存在?___(填“是”或“否”);
③设计简单实验验证原水样中可能存在的离子(写出实验步骤、现象和结论):___.
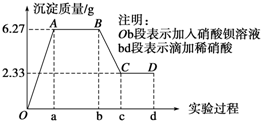
该水样为无色溶液,水样中一定不存在Fe3+、Cu2+;依据图象分析加入硝酸钡溶液生成沉淀,加入稀硝酸,沉淀部分溶解证明水样中一定含有SO42-、CO32-,又因为CO32-与Ag+、Ca2+、Mg2+发生反应生成沉淀不能大量存在,所以Ag+、Ca2+、Mg2+不存在;
n(SO42-)=
| 2.33g |
| 233g/mol |
| 6.27g-2.33g |
| 197g/mol |
原溶液中可能含有Cl-,依据电解质溶液中电荷守恒,阳离子K+一定存在;根据电荷守恒得到:0.01mol×2+0.02mol×2+n(Cl-)=n(K+)推知n(K+)≥0.06mol,
(1)根据分析可知,水样中一定含有的阴离子是SO42-、CO32-,
故答案为:SO42-、CO32-;
(2)依据电解质溶液中电荷守恒,阳离子K+一定存在,
故答案为:是;
(3)可能存在的离子是Cl-,验验证原水样中可能存在的离子的实验设计为:取少量水样与试管中,向试管中加入过量的硝酸钡溶液和稀硝酸,待沉淀完全和无气体生成后,向上层清液中滴加适量的硝酸银溶液,若生成白色沉淀,则原水样中 含有Cl-,若无白色沉淀生成,证明无Cl-存在,
故答案为:取少量水样与试管中,向试管中加入过量升温硝酸钡溶液和稀硝酸,待沉淀完全和无气体生成后,向上层清液中滴加适量的硝酸银溶液,若生成白色沉淀,则原水样中 含有Cl-,若无白色沉淀生成,证明无Cl-存在.

